近期,浙江大學劉旭、楊青課題組在超分辨顯微成像領域取得了重要研究進展。他們利用移頻成像原理,開創性地將發光納米線環作為局域光源與二維薄膜波導相耦合,巧妙地利用了納米光源小尺寸、大表體比、強光局域能力和強倏逝場等特點,首次實現了片上的大視場、遠場、無標記的超分辨顯微成像,分辨率較傳統顯微方法提升了5倍,且其視場比以往報道的無標記型遠場超分辨顯微方法擴展了2個數量級。
“2017中國光學十大進展”候選推薦
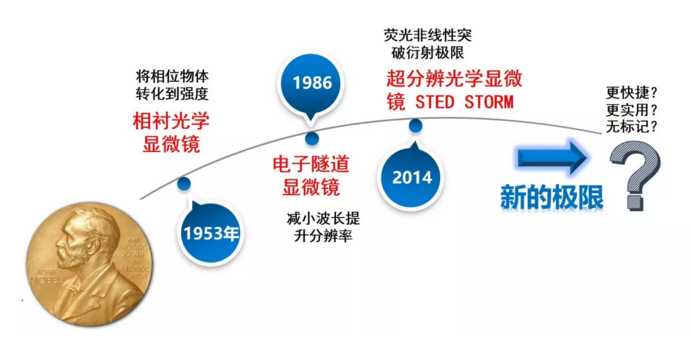
光學顯微鏡自16世紀發明以來,成為了人們探索微觀世界的重要工具。從列文虎克用自制的顯微鏡首次揭示微生物的存在到集成芯片微小缺陷的檢測,顯微技術的發展在近一個世紀的時間里突飛猛進,在1953年、1986年和2014年三次獲得了諾貝爾獎,極大地促進了生物醫學、物理和化學等領域的發展。
圖1 光學顯微成像的重要發展歷程
最初,人們認為,只要顯微鏡片的制作足夠精細,理論上可以觀察到任何微小的尺寸。然而,19世紀末,德國物理學家恩斯特·阿貝發現了“衍射極限”的存在,即光作為一種波,它的聚焦能力會受光學系統的孔徑(Numerical aperture,NA)和光波長的限制,聚焦光斑的尺寸不可能小于(0.61×λ)/ NA。這一特性限制了在可見光波段顯微成像的分辨能力,使200 nm以下的微小結構無法被傳統的顯微方法觀察。而打破衍射極限,實現“超分辨成像”,對人類科學取得突破性發展至關重要,因而成為了國內外研究者孜孜以求的目標。
2014年諾貝爾化學獎頒給了Stefan W. Hell,Eric Betzig 和 William E. Moerner,以表彰他們發明的受激發射損耗顯微成像(Stimulated Emission Depletion(STED)microscopy)和單分子顯微成像(Single-molecule Microscopy)將熒光顯微鏡的分辨率提高到了納米量級,為生物和醫學的發展提供了有力的研究手段。這些技術首先利用特殊的熒光顆粒對生物組織進行染色標記,然后通過使用熒光顆粒的非線性效應而將距離很近的結構分辨開來。但同時,基于熒光標記樣品的成像方法對熒光顆粒和成像樣品都有著較為嚴格的要求,普適性不強,且遇到了成像速度慢、易引起生物體排異反應等瓶頸。所需要的顯微系統昂貴而復雜。
相比起來,非熒光標記的超分辨顯微方法在活體成像、多類樣品成像和快速成像等方面具有天然的優勢。然而其發展卻非常緩慢,難以滿足材料、信息、醫學和生物科學等領域在無標記樣品檢測方面的迫切需求。國際上多個知名課題組對其展開研究,微球接觸、極透鏡等技術相繼被發明,但仍面臨著光譜范圍單一、視場狹窄等限制。探索并發展寬視場、遠場且結構與相位均能快速成像的新型非熒光標記超分辨顯微方法成為人們關注的難點與熱點。
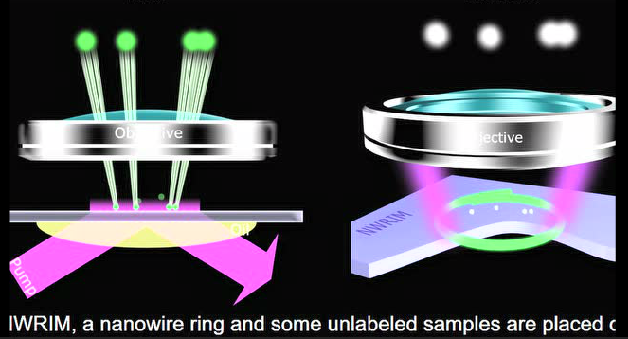
最近,該課題組利用移頻成像原理(如下視頻中所示),開創性地將發光納米線環作為局域光源,巧妙地利用其小尺寸、大表面積體積比、強光局域能力和強倏逝場等特點,并與低傳播損耗、高折射率的薄膜波導相耦合,首次實現了片上的大視場、遠場、無標記的超分辨顯微成像,分辨率較傳統顯微方法提升了5倍,且其視場比以往報道的無標記型遠場超分辨顯微方法擴展了2個數量級。
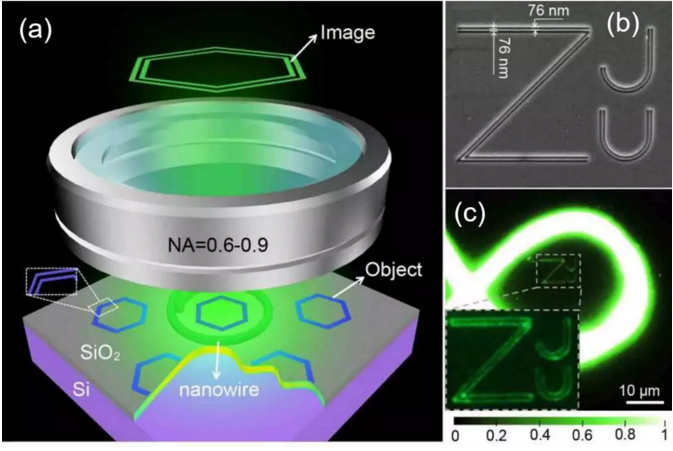
該方法是一種片上移頻顯微術,整個結構集成在一片毫米量級厚,厘米量級寬的硅片上,將之放入普通顯微系統代替傳統的載玻片,只需要激發片上的納米線光源發出熒光,即可使普通顯微鏡具備超分辨能力,實現從傳統顯微鏡到超分辨顯微鏡的飛躍提升。結構如圖2 (a)所示。圖2(b)為利用該方法觀察特征尺寸在幾十納米量級的“ZJU”圖案效果。
圖2 納米線環形照明顯微術機理示意圖(a)及“ZJU”結構觀察效果圖(b)
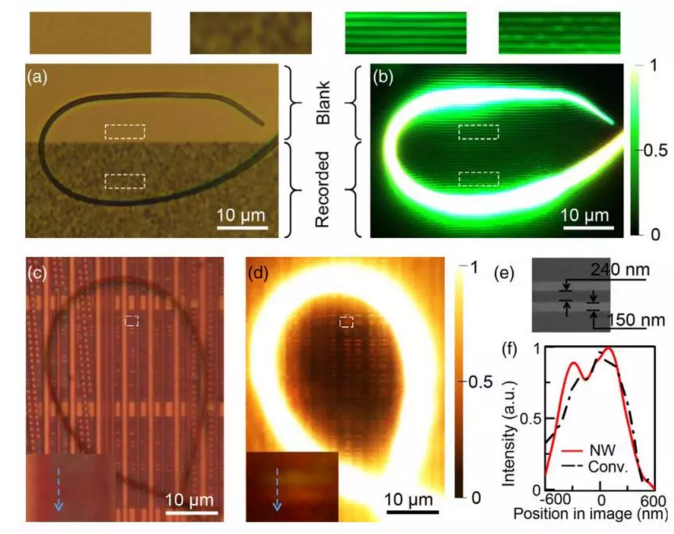
目前,該技術在集成芯片、藍光DVD、3T3-l1癌細胞等多類亞波長樣品上均得到驗證,顯示了其普適性強,使用方便的優點。圖3所示為使用該方法觀察藍光光碟和集成電路的效果圖。納米照明移頻顯微芯片的小尺寸、低功耗和高度兼容性使其在生物醫學、集成芯片和材料學等重要領域具有廣闊的應用前景,同時芯片化的設計可演化成主板型光學顯微鏡,為下一代光學顯微鏡提供顛覆性的設計理念。
圖3 NWRIM在藍光光碟和集成電路上的應用效果圖。(a) 藍光光碟的普通顯微成像;(b) 藍光光碟在納米線環照明下的成像;(c) 集成電路的普通顯微成像;(d) 集成電路在納米線環照明下的成像;(e) 子圖(c)與(d)中白色方框標示區域的電子顯微鏡照片;(f)子圖(c)與(d)中沿藍色虛線所描繪的成像強度分布。
![]()
![]()




 相關文章
相關文章 網友點評
網友點評
 熱門資訊
熱門資訊 精彩導讀
精彩導讀 關注我們
關注我們