腫瘤的靶向治療開創了腫瘤治療的新思路。納米藥物因其特定的尺寸,可利用腫瘤組織的EPR效應 (enhanced permeability and retention effect) 提高藥物對腫瘤組織的選擇性,在一定程度上實現了腫瘤的被動靶向治療。為進一步提高靶向效應,科學家們一直致力于納米藥物的靶向修飾,希望實現更高效的主動靶向治療。到目前為止,這種靶向修飾應用效果還十分有限。近年來,納米藥物領域開始利用一些納米材料的獨特性質,通過外界的刺激進行靶向腫瘤治療。比如,通過施加外部磁場引導具有磁性的納米藥物到達腫瘤部位進行治療。由于外界刺激方便可控的特點,越來越多的納米藥物研究者開始關注新型的腫瘤靶向策略。
國家納米科學中心陳春英和吳曉春兩個課題組近幾年密切合作,在金納米棒生物效應與安全性及生物醫學領域中的應用開展了深入系統的研究工作。他們在納米材料的光控釋藥、光熱逆轉腫瘤細胞耐藥性、增強腫瘤干細胞光熱響應的敏感性及多種策略聯合治療等方面取得一系列新發現,在腫瘤的個性化治療方向邁出了堅實的一步。
最近,他們在腫瘤的光熱刺激響應方面又取得了新突破,實現了與腫瘤組織的互動:將溫敏高分子材料修飾的金納米棒介孔二氧化硅納米復合物(Au@SiO2@polymer)通過尾靜脈注入小鼠體內。利用激光照射小鼠的腫瘤部位,腫瘤局部溫度升高引起血管通透性增加,溫敏納米復合物尺寸減小更加容易滲出血管,二者協同作用導致藥物更加有效地富集于腫瘤組織。因此,光刺激大幅度提高了藥物在腫瘤組織富集。在這種納米復合物中,金納米棒的光熱轉換性質與高分子材料的溫敏性質完美有機地結合在一起并實現了納米藥物光誘導的腫瘤主動靶向(圖1)。富集于腫瘤部位的納米復合物在激光照射下表現出熱療和化療(藥物釋放)兩種協同的治療效應,幾乎完全抑制腫瘤細胞的生長與轉移(圖2)。
由于激光的強弱、照射時間等可以方便且精確地控制,Au@SiO2@polymer提供了一種向腫瘤部位同時給藥和傳熱進行治療的理想載體。應用納米材料的獨特性質而實現的激光介導的腫瘤靶向治療代表了一種新型的抗腫瘤策略。
相關研究成果已發表于《美國化學會會志》( J. Am. Chem. Soc. 2014, 136, 7317?7326)。雜志審稿人認為:“光照控制的納米藥物主動靶向和藥物釋放是有趣而且頗具希望的多模態腫瘤治療技術。”
該研究得到了科技部、國家自然科學基金委和中國科學院的支持。
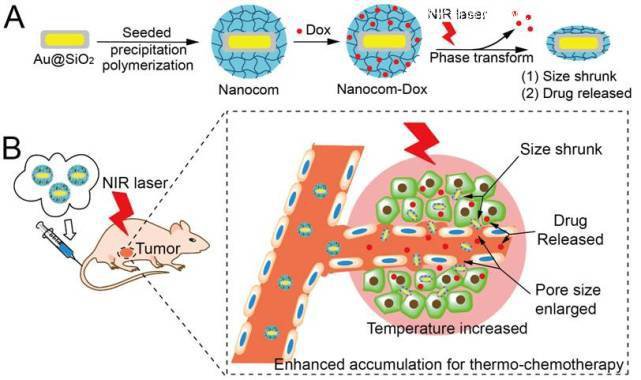
圖 1. 納米復合物Au@SiO2@polymer制備過程(A)與腫瘤靶向治療應用圖示(B)
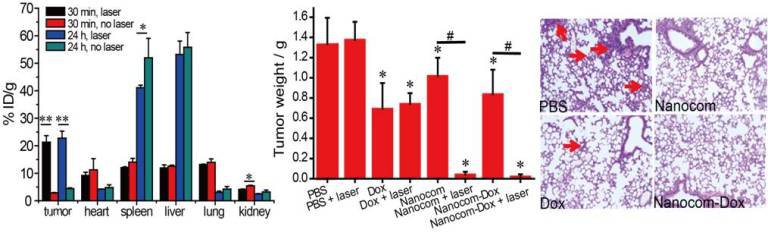 圖2. 納米復合物在激光照射下顯著富集于腫瘤組織,其產生的熱化療協同效應,有效抑制了腫瘤的生長與轉移。
圖2. 納米復合物在激光照射下顯著富集于腫瘤組織,其產生的熱化療協同效應,有效抑制了腫瘤的生長與轉移。
轉載請注明出處。







 相關文章
相關文章
 熱門資訊
熱門資訊
 精彩導讀
精彩導讀






























 關注我們
關注我們




